近日,珠江水产研究所水产养殖与营养研究室在罗非鱼Toll样受体介导的先天免疫机制研究方面取得新进展,相关研究论文《Nile tilapia Toll-like receptor 7 subfamily: Intracellular TLRs that recruit MyD88 as an adaptor and activate the NF-κB pathway in the immune response》和《Structurally diverse genes encode TLR13 in Nile tilapia: The two receptors can recognize Streptococcus 23S RNA and conduct signal transduction through MyD88》分别发表于JCR1区杂志《Developmental Comparative Immunology》(2020年JCR影响因子3.636)和JCR2区杂志《Molecular Immunology》(2020年JCR影响因子4.407)。该论文得到国家重点研发计划(2018YFD0900302)、财政部和农业农村部:国家现代农业产业技术体系专项资金(CARS-46)、广东省促渔业发展专项计划(粤农2019B8)资助。文章第一作者为高风英副研究员,通讯作者为卢迈新研究员。文章链接网址:https://doi.org/10.1016/j.dci.2021.104173https://doi.org/10.1016/j.molimm.2021.01.020
先天免疫在鱼类免疫中发挥重要作用。模式识别受体对病原微生物的识别是启动先天免疫反应的第一步。目前的模式识别受体有3大类,Toll样受体,NOD样受体和RIG-1样受体。本团队从Toll样受体家族成员入手进行罗非鱼先天免疫机制研究。论文1在获得TLR7,8,9三个成员基因序列的基础上,初步分析其信号转导机制:三个TLR成员均通过MyD88作为接头进行信号传导,参与NF-κB信号通路。论文2在弄清TLR13a和TLR13b可以识别无乳链球菌23s rRNA的基础上,检测到TLR13a和TLR13b可以与Myd88互作,并且发现TLR13a和TLR13b均可以增强myd88依赖的NF-κB,AP和IFN活性,由此得出结论:TLR13a和TLR13b的功能为:识别链球菌23s rRNA,然后通过Myd88进行信号转导至NF-κB以及AP和IFN,从而激活机体免疫反应。这些研究为进一步阐明罗非鱼的先天免疫机制奠定基础。
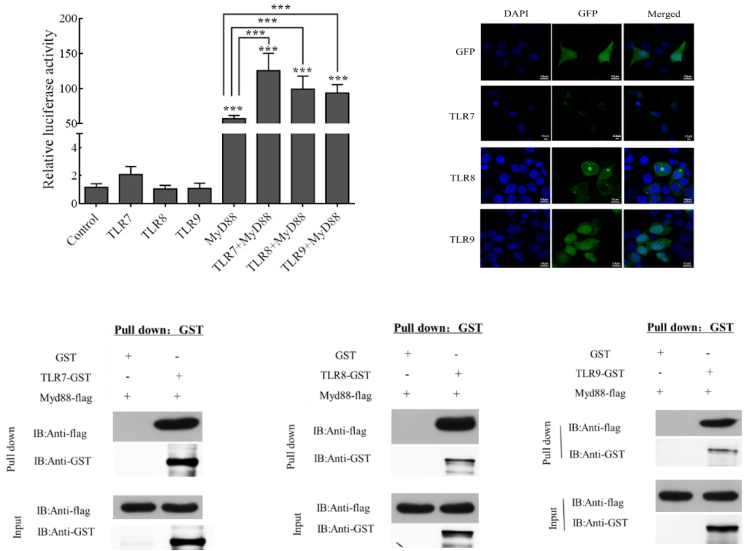
论文1相关图片:
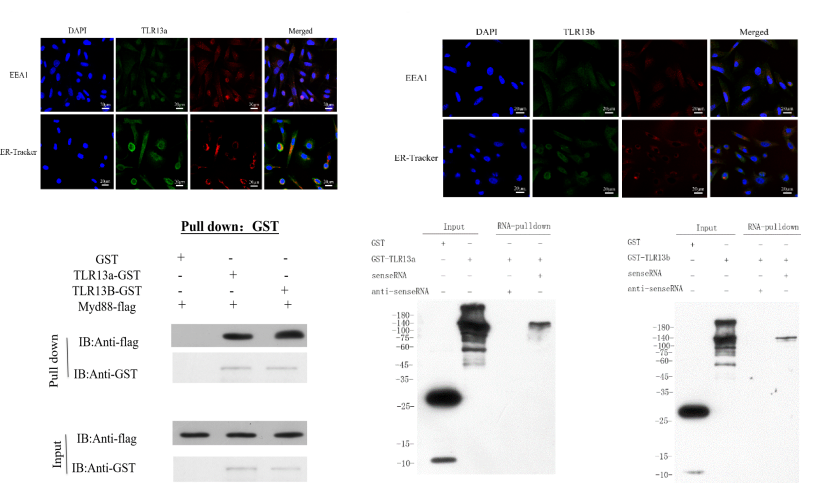
论文2相关图片: